经调整净亏损进一步扩大,“造血难”将成科济药业-B(02171)最大风险?
近日在2023美国癌症研究协会(AACR)年会上,CAR-T又凭借优异数据火了一把。
智通财经APP了解到,本次AACR大会上Allogene披露了其首个用于实体肿瘤的AlloCAR-T候选药物ALLO-316的最新研究数据,该产品旨在通过靶向CD70来治疗肾细胞癌(RCC)。最新数据显示,在10名表达CD70的患者中,ALLO-316的疾病控制率(DCR)达到100%,且安全性总体可控。
关键是这款产品运用的是Allogene的下一代通用CAR-T细胞平台技术Dagger™。
一直以来,通用CAR-T技术的研究进展都备受业界关注,在于传统自体CAR-T存在细胞制备工艺复杂、耗时长、成本高等问题。也正是基于以上自体CAR-T细胞的缺陷,科学家们提出了通用型CAR-T(UCART)细胞的概念。
介于目前出现的传统CAR-T产品上市后商业化困难的问题,市场对通用型CAR-T产品的出现更加期待。而在港股市场,科济药业-B(02171)作为一家同时开发传统CAR-T和通用型CAR-T产品的公司,其研发进展自然会受到市场重点关注。
股价“随波逐流”的背后
去年年5月10日,科济药业发布公告,其重磅产品CT041的研究者发起试验的期中分析结果在NatureMedicine上发表。结果显示,CT041整体耐受性良好且安全性风险可控。
在积极的研发成果带动下,科济药业次日股价收涨6.52%,并正式开启为期2个月的主升浪。智通财经APP观察到,科济药业股价在8月份逆市迎来一波反弹,并在8月26日将最高股价定格在每股20.65港元,较5月10日的最低点9.68港元上涨113.32%。
不过随着科济药业股价来到近5个月以来的新高,也正式宣布中期业绩炒作迎来尾声。自8月29日起,科济药业股价一路向下,截至9月19日已跌至最低13.04港元,15个交易日内较最高点回落36.85%。
从科济药业的这轮股价起伏来看,市场对公司的估值评判锚点依然较为清晰,公司股价上涨主要靠阶段性披露的研发成果驱动。
去年10月,港股18A板块开始整体向上反攻为港股医药行业带来一丝暖流。在这一趋势下,科济药业的股价从10月最低的9.2港元股价一路涨至1月最高的21.86港元,涨幅达到137.6%。但一如去年8月末,科济药业后续股价再度波动下跌,3个月内股价再度跌回11.82港元。
结合此前公司披露的2022年年报,公司全年净亏损约人民币8.92亿元,同比收窄81.19%;经调整净亏损约8.48亿元,同比增长54.57%。
从费用端来看,科济药业经调整净亏损扩大的主因便是研发投入增长。公司当期研发投入为6.8亿元,同比增长35.59%。
另外,截至2022年12月31日, 现金及现金等价物为人民币22.68亿元, 较截至2021年12月31日的人民币30.07亿元(包括原到期日3个月至12个月的定期存款)减少人民币7.39亿元。
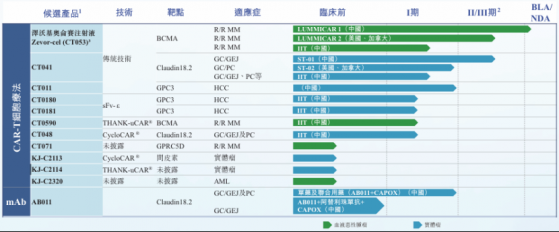
从研发进展来看,当前科济药业科济药业已自主开发了12款差异化候选产品,其中包括11款CAR-T细胞疗法和1款mAb产品,涵盖常规型、新一代CAR-T技术及同种异体疗法。
其中,其中,CT053作为科济药业的一款靶向BCMA用于治疗复发/难治多发性骨髓瘤(R/RMM)的自体CAR-T细胞核心候选产品,在去年10月,其NDA申请已获NMPA受理,并将其纳入优先审评。其在美国及加拿大进行的2期临床试验的入组正在进行中,其在美国也有望于2024年BLA。
与此同时,科济药业的另一款潜在全球同类首创的靶向Claudin18.2蛋白的自体CAR-T细胞候选产品CT041在去年上半年的2022ASCO年会公布的临床结果中展现了其显著的疗效与安全性。
目前CT041正在国内开展GC/GEJ确证性II期临床,其作为世界上第一款也是唯一一款进入II期临床试验的治疗实体瘤的CAR-T药物,正在中国、美国和加拿大开展多项针对胃癌、胰腺癌的临床试验。根据公司年报披露,科济药业计划在2024H1向NMPA提交NDA,CT041在美国的2期临床试验计划也于2023年上半年启动。凭借以上研发进度,CT041也有望成为全球第一款获批上市的实体瘤CAR-T药物。
简言之,从研发进度来看,CT053和CT041将先后成为科济药业首批实现商业化的产品。
但值得一提的是,以上两款产品均为运用传统自体技术的CAR-T产品,若参考目前全球及中国已上市CAR-T产品的商业化情况,CT053和CT041的商业化路径能否顺利打通似乎还有待验证,这或许也是影响科济药业股价波动的重要因素之一。
来自商业化的挑战
据智通财经APP了解,目前全球8款CAR-T上市,国产独占2席。2022年,两款国产获批上市的CAR-T疗法迎来了首个完整的商业化年度。其商业化成绩或许会在一定程度直接影响自体CAR-T产品商业化的市场信心。
不过随着财报季的结束,市场发现国内CAR-T产品的销售情况并不理想。以奕凯达为例,根据此前数据,截至2022年2月,约100名r/rLBCL患者进入奕凯达治疗流程;根据2022年最新数据,截至2023年1月,奕凯达已治疗近300名r/rLBCL患者。也就是说,2022年该产品至多治疗200例患者。
其背后主要问题在于,与其他创新药不同,传统自体CAR-T产品的成本较高,主要源于其需要个性化制备、较贵的进口载体等材料以及产品制备量太少无法形成规模效应。
而采用传统自体CAR-T技术的科济药业CT053和CT041或也将面临着跟国产已上市CAR-T产品一样“叫好不叫座”的商业化局面。
以CT053为例,其当前主要的适应症是多发性骨髓瘤(multiplemyeloma,MM),是全球第二大常见的血液恶性肿瘤。多药耐药和复发问题为MM当前治疗难题。这两大因素导致R/RMM成为治疗MM的研发重点,市场空间广阔。
数据显示,全球MM治疗市场将于2024年达395亿美元并在2030年达到473亿美元;中国MM治疗市场的规模将于2024年及2030年分别达24亿美元及39亿美元。
根据临床实验数据显示,CT053客观缓解率及三级以上CRS体现的有效性和安全性均优于海外竞品。
不过患者除了CT053还有多种药物治疗选择。
智通财经APP了解到,在中国多发性骨髓瘤治疗指南(2022年修订)中针对MM患者的治疗药物中,部分产品2022年全适应症销售额达到了9亿元以上。
其中唑来膦酸是治疗MM的辅助药物,其在2022年实现了14.68亿元收入,属于指南中MM治疗相关药物中销售额最高的产品。
除此之外,作为免疫抑制剂的来那度胺实现了11.39亿元的收入,传统药物地塞米松的零售终端实现2.36亿元收入,医院终端前三季度实现6.72亿元收入。单克隆抗体药物中,达雷妥尤单抗2022年零售终端实现2.58亿元收入,医院终端2022前三季度实现6.94亿元。
这也就表示,在临床疗效和安全性数据均表现较佳的情况下,上市后定价将成为制约CT053商业化的关键因素之一。
由此投资者可以清晰看到,目前科济药业的研发重心主要还是放在CT053、CT041等具有一定成熟技术的产品上,也就是说推动核心产品商业化是其主要目标。相较之下,譬如实体瘤增强型CycloCAR-T、基于同种异体THANK-uCAR-T平台研发的CT0590尚处在临床前研究或临床I期阶段,离商业化还有很远的距离。
